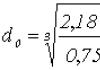Дисперсными называют гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в объеме другого.
То вещество, которое присутствует в меньшем количестве и распределено в объеме другого, называют дисперсной фазой . Она может состоять из нескольких веществ.
Вещество, присутствующее в большем количестве, в объеме которого распределена дисперсная фаза, называют дисперсионной средой . Между ней и частицами дисперсной фазы существует поверхность раздела, поэтому дисперсные системы называют гетерогенными (неоднородными).
И дисперсионную среду, и дисперсную фазу могут представлять вещества, находящиеся в различных агрегатных состояниях − твердом, жидком и газообразном.
В зависимости от сочетания агрегатного состояния дисперсионной среды и дисперсной фазы можно выделить 8 видов таких систем.
По величине частиц веществ, составляющих дисперсную фазу, дисперсные системы делят на грубодисперсные (взвеси) с размерами частиц более 100 нм и тонкодисперсные (коллоидные растворы или коллоидные системы) с размерами частиц от 100 до 1 нм. Если же вещество раздроблено до молекул или ионов размером менее 1 нм, образуется гомогенная система − раствор . Она однородна (гомогенна), поверхности раздела между частицами дисперсной фазы и средой нет.
Уже беглое знакомство с дисперсными системами и растворами показывает, насколько они важны в повседневной жизни и в природе (см. таблицу).
Таблица. Примеры дисперсных систем
| Дисперсионная среда | Дисперсная фаза | Примеры некоторых природных и бытовых дисперсных систем |
| Газ | Жидкость | Туман, попутный газ с капельками нефти, карбюраторная смесь в двигателях автомобилей (капельки бензина в воздухе), аэрозоли |
| Твердое вещество | Пыли в воздухе, дымы, смог, самумы (пыльные и песчаные бури), аэрозоли | |
| Жидкость | Газ | Шипучие напитки, пены |
| Жидкость | Эмульсии. Жидкие среды организма (плазма крови, лимфа, пищеварительные соки), жидкое содержимое клеток (цитоплазма, кариоплазма) | |
| Твердое вещество | Золи, гели, пасты (кисели, студни, клеи). Речной и морской ил, взвешенные в воде; строительные растворы | |
| Твердое вещество | Газ | Снежный наст с пузырьками воздуха в нем, почва, текстильные ткани, кирпич и керамика, поролон, пористый шоколад, порошки |
| Жидкость | Влажная почва, медицинские и косметические средства (мази, тушь, помада и т. д.) | |
| Твердое вещество | Горные породы, цветные стекла, некоторые сплавы |
Судите сами: без нильского ила не состоялась бы великая цивилизация Древнего Египта; без воды, воздуха, горных пород и минералов вообще бы не существовала живая планета − наш общий дом − Земля; без клеток не было бы живых организмов и т. д.
Если все частицы дисперсной фазы имеют одинаковые размеры, то такие системы называют монодисперсными (рис. 1, а и б). Частицы дисперсной фазы неодинакового размера образуют полидисперсные системы (рис.1, в).
Рис. 1. Свободнодисперсные системы: корпускулярно − (а-в), волокнисто − (г) и пленочно-дисперсные − (д); а, б − монодисперсные; в − полидисперсная система.
Дисперсные системы могут быть свободнодисперсными (рис. 1) и связнодисперсными (рис. 2, а − в) в зависимости от отсутствия или наличия взаимодействия между частицами дисперсной фазы. К свободнодисперсным системам относятся аэрозоли, разбавленные суспензии и эмульсии. Они текучи, в этих системах частицы дисперсной фазы не имеют контактов, участвуют в беспорядочном тепловом движении, свободно перемещаются под действием силы тяжести. Связнодисперсные системы − твердообразны; они возникают при контакте частиц дисперсной фазы, приводящем к образованию структуры в виде каркаса или сетки. Такая структура ограничивает текучесть дисперсной системы и придает ей способность сохранять форму. Порошки, концентрированные эмульсии и суспензии (пасты), пены, гели – примеры связнодисперсных систем. Сплошную массу вещества могут пронизывать поры и капилляры, образующие капиллярно-дисперсные системы (кожа, картон, ткани, древесина).

Рис. 3. Связнодисперсные (а-в) и капиллярно-дисперсные (г, д) системы: гель (а), коагулянт с плотной (б) и рыхлой – арочной (в) структурой.
Дисперсные системы, в соответствии с их промежуточным положением между миром молекул и крупных тел, могут быть получены двумя путями: методами диспергирования, т. е. измельчения крупных тел, и методами конденсации молекулярно- или ионнорастворенных веществ.
Под взаимодействием фаз дисперсных систем подразумевают процессы сольватации (гидратации в случае водных систем), т. е. образование сольватных (гидратных) оболочек из молекул дисперсионной среды вокруг частиц дисперсной фазы. Соответственно, по интенсивности взаимодействия между веществами дисперсной фазы и дисперсионной среды (только для систем с жидкой дисперсионной средой), по предложению Г. Фрейндлиха различают следующие дисперсные системы:
− Лиофильные (гидрофильные, если ДС – вода): мицеллярные растворы ПАВ, критические эмульсии, водные растворы некоторых природных ВМС, например, белков (желатина, яичного белка), полисахаридов (крахмала). Для них характерно сильное взаимодействие частиц ДФ с молекулами ДС. В предельном случае наблюдается полное растворение. Лиофильные дисперсные системы образуются самопроизвольно вследствие процесса сольватации. Термодинамически агрегативно устойчивы.
− Лиофобные (гидрофобные, если ДС – вода): эмульсии, суспензии, золи. Для них характерно слабое взаимодействие частиц ДФ с молекулами ДС. Самопроизвольно не образуются, для их образования необходимо затратить работу. Термодинамически агрегативно неустойчивы (т. е. имеют тенденцию к самопроизвольной агрегации частиц дисперсной фазы), их относительная устойчивость (так называемая метастабильность ) обусловлена кинетическими факторами (т. е. низкой скоростью агрегации).
3. Взвеси.
Взвеси – это дисперсные системы, в которых размер частицы фазы более 100 нм. Это непрозрачные системы, отдельные частицы которых можно заметить невооруженным глазом. Дисперсная фаза и дисперсная среда легко разделяются отстаиванием, фильтрованием. Такие системы разделяются на:
1. Эмульсии (и среда, и фаза – нерастворимые друг в друге жидкости). Из воды и масла можно приготовить эмульсию длительным встряхиванием смеси. Это хорошо известные вам молоко, лимфа, водоэмульсионные краски и т.д.
2. Суспензии (среда – жидкость, фаза – нерастворимое в ней твердое вещество).Чтобы приготовить суспензию, надо вещество измельчить до тонкого порошка, высыпать в жидкость и хорошо взболтать. Со временем частица выпадут на дно сосуда. Очевидно, чем меньше частицы, тем дольше будет сохраняться суспензия. Это строительные растворы, взвешенный в воде речной и морской ил, живая взвесь микроскопических живых организмов в морской воде – планктон, которым питаются гиганты – киты, и т.д.
3. Аэрозоли взвеси в газе (например, в воздухе) мелких частиц жидкостей или твердых веществ. Различаются пыли, дымы, туманы. Первые два вида аэрозолей представляют собой взвеси твердых частиц в газе (более крупные частицы в пылях), последний – взвесь капелек жидкости в газе. Например: туман, грозовые тучи – взвесь в воздухе капелек воды, дым – мелких твердых частиц. А смог, висящий над крупнейшими городами мира, также аэрозоль с твердой и жидкой дисперсной фазой. Жители населенных пунктов вблизи цементных заводов страдают от всегда висящей в воздухе тончайшей цементной пыли, образующейся при размоле цементного сырья и продукта его обжига – клинкера. Дым заводских труб, смоги, мельчайшие капельки слюны, вылетающих изо рта больного гриппом, также вредные аэролози. Аэрозоли играют важную роль в природе, быту и производственной деятельности человека. Скопление облаков, обработка полей химикатами, нанесение лакокрасочных покрытий при помощи пульверизатора, лечение дыхательных путей (ингаляция) – примеры тех явлений и процессов, где аэрозоли приносят пользу. Аэрозоли – туманы над морским прибоем, вблизи водопадов и фонтанов, возникающая в них радуга доставляет человеку радость, эстетическое удовольствие.
Для химии наибольшее значение имеют дисперсные системы, в которых средой является вода и жидкие растворы.
Природная вода всегда содержит растворенные вещества. Природные водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами. Сложные процессы жизнедеятельности, происходящие в организмах человека и животных, также протекают в растворах. Многие технологические процессы в химической и других отраслях промышленности, например получение кислот, металлов, бумаги, соды, удобрений, протекают в растворах.
4. Коллоидные системы.
Коллоидные системы (в переводе с греческого “колла” – клей, “еидос” вид клееподобные) – это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти частицы не видны невооруженным глазом, и дисперсная фаза и дисперсная среда в таких системах отстаиванием разделяются с трудом.
Из курса общей биологии вам известно, что частицы такого размера можно обнаружить при помощи ультрамикроскопа, в котором используется принцип рассеивания света. Благодаря этому коллоидная частица в нем кажется яркой точкой на темном фоне.
Их подразделят на золи (коллоидные растворы) и гели (студни).
1. Коллоидные растворы , или золи . Это большинство жидкостей живой клетки (цитоплазма, ядерный сок – кариоплазма, содержимое органоидов и вакуолей). И живого организма в целом (кровь, лимфа, тканевая жидкость, пищеварительные соки и т.д.) Такие системы образуют клеи, крахмал, белки, некоторые полимеры.
Коллоидные растворы могут быть получены в результате химических реакций; например, при взаимодействии растворов силикатов калия или натрия (“растворимого стекла”) с растворами кислот образуется коллоидный раствор кремниевой кислоты. Золь образуется и при гидролизе хлорида железа (III) в горячей воде.
Характерное свойство коллоидных растворов – их прозрачность. Коллоидные растворы внешне похожи на истинные растворы. Их отличают от последних по образующейся “светящейся дорожке” – конусу при пропускании через них луча света. Это явление называют эффектом Тиндаля. Более крупные, чем в истинном растворе, частицы дисперсной фазы золя отражают свет от своей поверхности, и наблюдатель видит в сосуде с коллоидным раствором светящийся конус. В истинном растворе он не образуется. Аналогичный эффект, но только для аэрозольного, а не жидкого коллоида, вы можете наблюдать в лесу и в кинотеатрах при прохождении луча света от киноаппарата через воздух кинозала.

Пропускание луча света через растворы:
а – истинный раствор хлорида натрия;
б – коллоидный раствор гидроксида железа (III).
Частицы дисперсной фазы коллоидных растворов нередко не оседают даже при длительном хранении из-за непрерывных соударений с молекулами растворителя за счет теплового движения. Они не слипаются и при сближении друг с другом из-за наличия на их поверхности одноименных электрических зарядов. Это объясняется тем, что вещества в коллоидном, т.е., в мелкораздробленном, состоянии обладают большой поверхностью. На этой поверхности адсорбируются либо положительно, либо отрицательно заряженные ионы. Например, кремниевая кислота адсорбирует отрицательные ионы SiO 3 2- , которых в растворе много вследствие диссоциации силиката натрия:

Частицы же с одноименными зарядами взаимно отталкиваются и поэтому не слипаются.
Но при определенных условиях может происходить процесс коагуляции. При кипячении некоторых коллоидных растворов происходит десорбция заряженных ионов, т.е. коллоидные частицы теряют заряд. Начинают укрупняться и оседают. Тоже самое наблюдается при приливании какого-либо электролита. В этом случае коллоидная частица притягивает к себе противоположно заряженный ион и ее заряд нейтрализуется.
Коагуляция – явление слипания коллоидных частиц и выпадения их в осадок – наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (клей, яичный белок) или при изменении кислотно-щелочной среды раствора.
2. Гели или студни представляют собой студенистые осадки, образующиеся при коагуляции золей. К ним относят большое количество полимерных гелей, столь хорошо известные вам кондитерские, косметические и медицинские гели (желатин, холодец, мармелад, хлеб, мясо, джем, желе, мармелад, кисель, сыр, творог, простокваша, торт “Птичье молоко”) и конечно же бесконечное множество природных гелей: минералы (опал), тела медуз, хрящи, сухожилия, волосы, мышечная и нервная ткани и т.д. Историю развития на Земле можно одновременно считать историей эволюции коллоидного состояния вещества. Со временем структура гелей нарушается (отслаивается) – из них выделяется вода. Это явление называют синерезисом .
Студни − это структурированные системы со свойствами эластичных твердых тел. Студнеобразное состояние вещества можно рассматривать как промежуточное между жидким и твердым состоянием.
Студни высокомолекулярных веществ могут быть получены в основном двумя путями: методом образования студней из растворов полимеров и методом набухания сухих высокомолекулярных веществ в соответствующих жидкостях.
Процесс перехода раствора полимера или золя в студень называется студнеобразованием . Студнеобразование связано с увеличением вязкости и замедлением броуновского движения и заключается в объединении частиц дисперсной фазы в форме сетки или ячеек и связывании при этом всего растворителя.
На процесс студнеобразования существенно влияет природа растворенных веществ, форма их частиц, концентрация, температура, время процесса и примеси других веществ, особенно электролитов.
На основании свойств студни делят на две большие группы:
а) эластичные, или обратимые, получаемые из высокомолекулярных веществ;
б) хрупкие, или необратимые, получаемые из неорганических гидрофобных золей.
Как уже говорилось, студни высокомолекулярных веществ могут быть получены не только методом студнеобразования растворов, но и методом набухания сухих веществ. Ограниченное набухание заканчивается образованием студня и не переходит в растворение, а при неограниченном набухании студень - промежуточная стадия на пути к растворению.
Для студней характерен ряд свойств твердых тел: они сохраняют форму, обладают упругими свойствами и эластичностью. Однако их механические свойства определяются концентрацией и температурой.
При нагревании студни переходят в вязкотекучее состояние. Этот процесс называется плавлением. Он обратим, так как при охлаждении раствор снова образовывает студень.
Многие студни способны разжижаться и переходить в растворы при механическом воздействии (перемешивание, встряхивание). Этот процесс обратим, так как в состоянии покоя через некоторое время раствор образовывает студень. Свойство студней многократно изотермически разжижаться при механических воздействиях и образовывать студень в состоянии покоя называется тиксотропией . К тиксотропным изменениям способны, например, шоколадная масса, маргарин, тесто.
Имея в своем составе огромное количество воды, студни, кроме свойств твердых тел, обладают и свойствами жидкого тела. В них могут протекать различные физико-химические процессы: диффузия, химические реакции между веществами.
Свежеприготовленные студни с течением времени подвергаются изменениям, так как процесс структурирования в студне продолжается. При этом на поверхности студня начинают появляться капельки жидкости, которые, сливаясь, образуют жидкую среду. Образующаяся дисперсионная среда является разбавленным раствором полимера, а дисперсная фаза – студнеобразная фракция. Такой самопроизвольный процесс разделения студня на фазы, сопровождающийся изменением объема студия, называет синерезисом (отмоканием).
Синерезис рассматривается как продолжение процессов, обусловливающих образование студня. Скорость синерезиса различных студней различна и зависит в основном от температуры и концентрации.
Синерезис у студней, образованных полимерами, частично обратим. Иногда достаточно нагревания, чтобы студень, претерпевший синерезис, вернуть в исходное состояние, В кулинарной практике этим способом пользуются, например, для освежения каш, пюре, черствого хлеба. Если при хранении студней возникают химические процессы, то синерезис усложняется и его обратимость теряется, происходит старение студня. При этом студень теряет способность удерживать связанную воду (черствение хлеба). Практическое значение синерезиса довольно велико. Чаще всего синерезис в быту и промышленности нежелателен. Это черствение хлеба, отмокание мармелада, желе, карамели, фруктовых джемов.
5. Растворы высокомолекулярных веществ.
Полимеры, подобно низкомолекулярным веществам, в зависимости от условий получения раствора (природа полимера и растворителя, температура и др.) могут образовывать как коллоидные, так и истинные растворы. В связи с этим принято говорить о коллоидном или истинном состоянии вещества в растворе. Мы не будем касаться систем «полимер – растворитель» коллоидного типа. Рассмотрим только растворы полимеров молекулярного типа. Следует отметить, что вследствие больших размеров молекул и особенностей их строения, растворы ВМС обладают рядом специфических свойств:
1. Равновесные процессы в растворах ВМС устанавливаются медленно.
2. Процессу растворения ВМС, как правило, предшествует процесс набухания.
3. Растворы полимеров не подчиняются законам идеальных растворов, т.е. законам Рауля и Вант-Гоффа.
4. При течении растворов полимеров возникает анизотропия свойств (неодинаковые физические свойства раствора в разных направлениях) за счет ориентации молекул в направлении течения.
5. Высокая вязкость растворов ВМС.
6. Молекулы полимеров, благодаря большим размерам, проявляют склонность к ассоциации в растворах. Время жизни ассоциатов полимеров более длительное, чем ассоциатов низкомолекулярных веществ.
Процесс растворения ВМС протекает самопроизвольно, но в течение длительного времени, и ему часто предшествует набухание полимера в растворителе. Полимеры, макромолекулы которых имеют симметричную форму, могут переходить в раствор, предварительно не набухая. Например, гемоглобин, печеночный крахмал – гликоген при растворении почти не набухают, а растворы этих веществ не обладают высокой вязкостью даже при сравнительно больших концентрациях. В то время, как вещества с сильно асимметрическими вытянутыми молекулами при растворении очень сильно набухают (желатин, целлюлоза, натуральный и синтетические каучуки).
Набухание – это увеличение массы и объема полимера за счет проникновения молекул растворителя в пространственную структуру ВМС.
Различают два вида набухания: неограниченное, заканчивающееся полным растворением ВМС (например, набухание желатины в воде, каучука в бензоле, нитроцеллюлозы в ацетоне) и ограниченное , приводящее к образованию набухшего полимера – студня (например, набухание целлюлозы в воде, желатина в холодной воде, вулканизованного каучука в бензоле).
Дисперсные системы
Чистые
вещества в природе встречаются очень редко. Смеси разных веществ в различных
агрегатных состояниях могут образовывать гетерогенные и гомогенные системы -
дисперсные системы и растворы.
Дисперсными
называют гетерогенные системы, в которых одно вещество в виде очень мелких
частиц равномерно распределено в объеме другого.
То вещество, которое присутствует в меньшем количестве и распределено в объеме
другого, называют дисперсной фазой
. Она может состоять из нескольких веществ.
Вещество, присутствующее в большем количестве, в объеме которого распределена
дисперсная фаза, называют дисперсионной средой
. Между ней и
частицами дисперсной фазы существует поверхность раздела, поэтому дисперсные
системы называют гетерогенными (неоднородными).
И дисперсионную среду, и дисперсную фазу могут представлять вещества,
находящиеся в различных агрегатных состояниях - твердом, жидком и газообразном.
В зависимости от сочетания агрегатного состояния дисперсионной среды и
дисперсной фазы можно выделить 9 видов таких систем.
По величине частиц веществ, составляющих дисперсную фазу, дисперсные системы делят на грубодисперсные (взвеси) с размерами частиц более 100 нм и тонкодисперсные (коллоидные растворы или коллоидные системы) с размерами частиц от 100 до 1 нм. Если же вещество раздроблено до молекул или ионов размером менее 1 нм, образуется гомогенная система - раствор. Она однородна (гомогенна), поверхности раздела между частицами и средой нет.
Уже беглое знакомство с дисперсными системами и растворами показывает, насколько они важны в повседневной жизни и в природе.
Судите
сами: без нильского ила не состоялась бы великая цивилизация Древнего Египта;
без воды, воздуха, горных пород и минералов вообще бы не существовала живая
планета - наш общий дом - Земля; без клеток не было бы живых организмов и т. д.
Классификация дисперсных систем и растворов
Взвеси
Взвеси
- это дисперсные системы, в которых размер частиц фазы более 100 нм. Это
непрозрачные системы, отдельные частицы которых можно заметить невооруженным
глазом. Дисперсная фаза и дисперсионная среда легко разделяются отстаиванием.
Такие системы разделяют на:
1) эмульсии
(и среда, и фаза - нерастворимые друг в друге
жидкости). Это хорошо известные вам молоко, лимфа, водоэмульсионные краски и т.
д.;
2) суспензии
(среда - жидкость, а фаза -
нерастворимое в ней твердое вещество). Это строительные растворы (например,
«известковое молоко» для побелки), взвешенный в воде речной и морской ил, живая
взвесь микроскопических живых организмов в морской воде - планктон, которым питаются
гиганты-киты, и т. д.;
3) аэрозоли
- взвеси в газе (например,
в воздухе) мелких частиц жидкостей или твердых веществ. Различают пыли, дымы,
туманы. Первые два вида аэрозолей представляют собой взвеси твердых частиц в
газе (более крупные частицы в пылях), последний - взвесь мелких капелек
жидкости в газе. Например, природные аэрозоли: туман, грозовые тучи - взвесь в
воздухе капелек воды, дым - мелких твердых частиц. А смог, висящий над
крупнейшими городами мира, также аэрозоль с твердой и жидкой дисперсной фазой.
Жители населенных пунктов вблизи цементных заводов страдают от всегда висящей в
воздухе тончайшей цементной пыли, образующейся при размоле цементного сырья и
продукта его обжига - клинкера. Аналогичные вредные аэрозоли - пыли - имеются и
в городах с металлургическими производствами. Дым заводских труб, смоги,
мельчайшие капельки слюны, вылетающие изо рта больного гриппом, также вредные
аэрозоли.
Аэрозоли играют важную роль в природе, быту и производственной деятельности
человека. Скопления облаков, обработка полей химикатами, нанесение
лакокрасочных покрытий при помощи пульверизатора, распыление топлив, выработка
сухих молочных продуктов, лечение дыхательных путей (ингаляция) - примеры тех
явлений и процессов, где аэрозоли приносят пользу. Аэрозоли - туманы над
морским прибоем, вблизи водопадов и фонтанов, возникающая в них радуга
доставляет человеку радость, эстетическое удовольствие.
Для химии наибольшее значение имеют дисперсные системы, в которых средой
является вода и жидкие растворы.
Природная вода всегда содержит растворенные вещества. Природные водные растворы
участвуют в процессах почвообразования и снабжают растения питательными
веществами. Сложные процессы жизнедеятельности, происходящие в организмах
человека и животных, также протекают в растворах. Многие технологические
процессы в химической и других отраслях промышленности, например получение
кислот, металлов, бумаги, соды, удобрений, протекают в растворах.
Коллоидные системы
Коллоидные системы
- это
такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти
частицы не видны невооруженным глазом, и дисперсная фаза и дисперсионная среда
в таких системах отстаиванием разделяются с трудом.
Их подразделяют на золи (коллоидные растворы) и гели (студни).
1.
Коллоидные растворы, или золи.
Это большинство жидкостей
живой клетки (цитоплазма, ядерный сок - кариоплазма, содержимое органоидов и
вакуолей) и живого организма в целом (кровь, лимфа, тканевая жидкость,
пищеварительные соки, гуморальные жидкости и т. д.). Такие системы образуют
клеи, крахмал, белки, некоторые полимеры.
Коллоидные растворы могут быть получены в результате химических реакций;
например, при взаимодействии растворов силикатов калия или натрия
(«растворимого стекла») с растворами кислот образуется коллоидный раствор
кремниевой кислоты. Золь образуется и при гидролизе хлорида железа (Ш) в
горячей воде. Коллоидные растворы внешне похожи на истинные растворы. Их
отличают от последних по образующейся «светящейся дорожке» - конусу при
пропускании через них луча света.
Частицы дисперсной фазы коллоидных растворов нередко не оседают даже при длительном хранении из-за непрерывных соударений с молекулами растворителя за счет теплового движения. Они не слипаются и при сближении друг с другом из-за наличия на их поверхности одноименных электрических зарядов. Но при определенных условиях может происходить процесс коагуляции.
Коагуляция - явление слипания коллоидных частиц и выпадения их в осадок - наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (клей, яичный белок) или при изменении кислотно-щелочной среды раствора.
2.
Гели
, или студни,
представляющие собой студенистые осадки, образующиеся при коагуляции золей. К
ним относят большое количество полимерных гелей, столь хорошо известные вам
кондитерские, косметические и медицинские гели (желатин, холодец, желе,
мармелад, торт «Птичье молоко») и конечно же бесконечное множество природных
гелей: минералы (опал), тела медуз, хрящи, сухожилия, волосы, мышечная и
нервная ткани и т. д. Историю развития жизни на Земле можно одновременно
считать историей эволюции коллоидного состояния вещества. Со временем структура
гелей нарушается - из них выделяется вода. Это явление называют синерезисом
.
Растворы
Раствором называют
гомогенную
систему, состоящую из двух и более веществ.
Растворы всегда однофазны, то есть представляют собой однородный газ, жидкость
или твердое вещество. Это связано с тем, что одно из веществ распределено в
массе другого в виде молекул, атомов или ионов (размер частиц менее 1 нм).
Растворы называют истинными
,
если требуется подчеркнуть их отличие от коллоидных растворов.
Растворителем считают то вещество, агрегатное состояние которого не изменяется
при образовании раствора. Например, вода в водных растворах поваренной соли,
сахара, углекислого газа. Если же раствор образовался при смешении газа с
газом, жидкости с жидкостью и твердого вещества с твердым, растворителем
считают тот компонент, которого больше в растворе. Так, воздух - это раствор
кислорода, благородных газов, углекислого газа в азоте (растворитель). Столовый
уксус, в котором содержится от 5 до 9% уксусной кислоты, представляет собой
раствор этой кислоты в воде (растворитель - вода). Но в уксусной эссенции роль
растворителя играет уксусная кислота, так как ее массовая доля составляет 70-
80%, следовательно, это раствор воды в уксусной кислоте.
При
кристаллизации жидкого сплава серебра и золота можно получить твердые растворы
разного состава.
Растворы
подразделяют на:
молекулярные
- это
водные растворы неэлектролитов - органических веществ (спирта, глюкозы,
сахарозы и т. д.);
молекулярно-ионные
- это
растворы слабых электролитов (азотистой, сероводородной кислот и др.);
ионные
- это растворы
сильных электролитов (щелочей, солей, кислот - NaOH, K 2 S0 4 ,
HN0 3 , НС1О 4).
Раньше существовали две точки зрения на природу растворения и растворов:
физическая и химическая. Согласно первой растворы рассматривали как
механические смеси, согласно второй - как нестойкие химические соединения
частиц растворенного вещества с водой или другим растворителем. Последняя
теория была высказана в 1887 г. Д. И. Менделеевым, который посвятил
исследованию растворов более 40 лет. Современная химия рассматривает
растворение как физико-химический процесс, а растворы как физико-химические
системы.
Более точное определение раствора таково:
Раствор
- гомогенная (однородная) система,
состоящая из частиц растворенного вещества, растворителя и продуктов их
взаимодействия.
Поведение и свойства растворов электролитов, как вы хорошо знаете, объясняет
другая важнейшая теория химии - теория электролитической диссоциации,
разработанная С. Аррениусом, развитая и дополненная учениками Д. И. Менделеева,
и в первую очередь И. А. Каблуковым.
Вопросы для закрепления:
1. Что такое дисперсные системы?
2. При повреждении кожи (ранке) наблюдается свертывание крови
- коагуляция золя. В чем сущность этого процесса? Почему это явление выполняет
защитную функцию для организма? Как называют болезнь, при которой свертывание
крови затруднено или не наблюдается?
3. Расскажите о значении различных дисперсных систем в быту.
4. Проследите эволюцию коллоидных систем в процессе развития
жизни на Земле.
Дисперсионные системы можно разделить по размеру частиц дисперсионной фазы. Если размер частиц составляет меньше одного нм – это молекулярно - ионные системы, от одного до ста нм - коллоидные, и более ста нм - грубодисперсные. Группу молекулярно дисперсных систем представляют растворы. Это однородные системы, которые состоят из двух или более веществ и являются однофазными. К ним относятся газ, твердое вещество или растворы. В свою очередь эти системы можно разделить на подгруппы:
- Молекулярные. Когда органические вещества, такие как глюкоза, соединяются с неэлектролитами. Такие растворы назвали истинными для того, чтобы можно было отличать от коллоидных. К ним относятся растворы глюкозы, сахарозы, спиртовые и другие.
- Молекулярно-ионные. В случае взаимодействия между собой слабых электролитов. В эту группу входят кислотные растворы, азотистые, сероводородные и другие.
- Ионные. Соединение сильных электролитов. Яркие представители - это растворы щелочей, солей и некоторых кислот.
Коллоидные системы
Коллоидные системы - это микрогетерогенные системы, в которых размеры коллоидных частиц варьируют от 100 до 1 нм. Они длительное время могут не выпадать в осадок за счет сольватной ионной оболочки и электрического заряда. При распределении в среде коллоидные растворы заполняют равномерно весь объем и делятся на золи и гели, которые в свою очередь представляют собой осадки в виде студня. К ним относятся раствор альбумина, желатина, коллоидные растворы серебра. Холодец, суфле, пудинги - это яркие коллоидной систем, встречающихся в повседневной жизни.
Грубодисперсные системы
Непрозрачные системы или взвеси, в которых мелкие ингредиенты частицы видны невооруженным глазом. В процессе отстаивания дисперсная фаза легко отделяется от дисперсной среды. Они подразделяются на суспензии, эмульсии, аэрозоли. Системы, в которых в жидкой дисперсионной среде размещаются твердое вещество с более крупными частицами, называются суспензиями. К ним относятся водные растворы крахмала и глины. В отличие от суспензий, эмульсии получаются в результате смешивания двух жидкостей, в которых одна капельками распределяется в другой. Примером эмульсии является смесь масла с водой, капельки жира в молоке. Если мелкие твердые или жидкие частицы распределяется в газе - это аэрозоли. По сути аэрозоль - это суспензия в газе. Одним из представителей аэрозоля на основе жидкости является туман - это большое количество мелких водяных капелек, взвешенных в воздухе. Твердотельный аэрозоль – дым или пыль - множественное скопление мелких твердых частиц также взвешенных в воздухе.
Разделы: Химия
Класс: 11
Изучив тему урока, вы узнаете:
- что такое дисперсные системы?
- какими бывают дисперсные системы?
- какими свойствами обладают дисперсные системы?
- значение дисперсных систем.
Чистые вещества в природе встречаются очень редко. Кристаллы чистых веществ – сахара или поваренной соли, например, можно получить разного размера – крупные и мелкие. Каков бы ни был размер кристаллов, все они имеют одинаковую для данного вещество внутреннюю структуру – молекулярную или ионную кристаллическую решетку.
В природе чаще всего встречаются смеси различных веществ. Смеси разных веществ в различных агрегатных состояниях могут образовывать гетерогенные и гомогенные системы. Такие системы мы будем называть дисперсными.
Дисперсной называется система, состоящая из двух или более веществ, причем одно из них в виде очень маленьких частиц равномерно распределено в объеме другого.
Вещество распадается на ионы, молекулы, атомы, значит “дробится” на мельчайшие частицы. “Дробление” > диспергирование, т.е. вещества диспергируют до разных размеров частиц видимых и невидимых.
Вещество, которое присутствует в меньшем количестве, диспергирует и распределено в объеме другого, называют дисперсной фазой. Она может состоять из нескольких веществ.
Вещество, присутствующее в большем количестве, в объеме которого распределена дисперсная фаза, называют дисперсной средой. Между ней и частицами дисперсной фазы существует поверхность раздела, поэтому дисперсные системы называются гетерогенными (неоднородными).
И дисперсную среду, и дисперсную фазу могут представлять вещества, находящиеся в различных агрегатных состояниях – твердом, жидком и газообразном.
В зависимости от сочетания агрегатного состояния дисперсной среды и дисперсной фазы можно выделить 9 видов таких систем.
Таблица
Примеры дисперсных систем
| Дисперсионная среда | Дисперсная фаза | Примеры некоторых природных и бытовых дисперсных систем |
| Газ | Газ | Всегда гомогенная смесь (воздух, природный газ) |
| Жидкость | Туман, попутный газ с капельками нефти, карбюраторная смесь в двигателях автомобилей (капельки бензина в воздухе), аэрозоли | |
| Твердое вещество | Пыли в воздухе, дымы, смог, самумы (пыльные и песчаные бури), аэрозоли | |
| Жидкость | Газ | Шипучие напитки, пены |
| Жидкость | Эмульсии. Жидкие среды организма (плазма крови, лимфа, пищеварительные соки), жидкое содержимое клеток (цитоплазма, кариоплазма) | |
| Твердое вещество | Золи, гели, пасты (кисели, студни, клеи). Речной и морской ил, взвешенные в воде; строительные растворы | |
| Твердое вещество | Газ | Снежный наст с пузырьками воздуха в нем, почва, текстильные ткани, кирпич и керамика, поролон, пористый шоколад, порошки |
| Жидкость | Влажная почва, медицинские и косметические средства (мази, тушь, помада и т. д.) | |
| Твердое вещество | Горные породы, цветные стекла, некоторые сплавы |
По величине частиц веществ, составляющих дисперсную фазу, дисперсные системы делятся на грубодисперсные (взвеси) с размерами частиц более 100 нм и тонкодисперсные (коллоидные растворы или коллоидные системы) с размерами частиц от 100 до 1 нм. Если же вещество раздроблено до молекул или ионов размером менее 1 нм, образуется гомогенная система – раствор . Она однородна, поверхности раздела между частицами и средой нет.
Дисперсные системы и растворы очень важны в повседневной жизни и в природе. Судите сами: без нильского ила не состоялась бы великая цивилизация Древнего Египта; без воды, воздуха, горных пород и минералов вообще бы не существовала живая планета – наш общий дом – Земля; без клеток не было бы живых организмов и т.д.
ВЗВЕСИ
Взвеси – это дисперсные системы, в которых размер частицы фазы более 100 нм. Это непрозрачные системы, отдельные частицы которых можно заметить невооруженным глазом. Дисперсная фаза и дисперсная среда легко разделяются отстаиванием, фильтрованием. Такие системы разделяются на:
- Эмульсии (и среда, и фаза – нерастворимые друг в друге жидкости). Из воды и масла можно приготовить эмульсию длительным встряхиванием смеси. Это хорошо известные вам молоко, лимфа, водоэмульсионные краски и т.д.
- Суспензии (среда – жидкость, фаза – нерастворимое в ней твердое вещество).Чтобы приготовить суспензию, надо вещество измельчить до тонкого порошка, высыпать в жидкость и хорошо взболтать. Со временем частица выпадут на дно сосуда. Очевидно, чем меньше частицы, тем дольше будет сохраняться суспензия. Это строительные растворы, взвешенный в воде речной и морской ил, живая взвесь микроскопических живых организмов в морской воде – планктон, которым питаются гиганты – киты, и т.д.
- Аэрозоли взвеси в газе (например, в воздухе) мелких частиц жидкостей или твердых веществ. Различаются пыли, дымы, туманы. Первые два вида аэрозолей представляют собой взвеси твердых частиц в газе (более крупные частицы в пылях), последний – взвесь капелек жидкости в газе. Например: туман, грозовые тучи – взвесь в воздухе капелек воды, дым – мелких твердых частиц. А смог, висящий над крупнейшими городами мира, также аэрозоль с твердой и жидкой дисперсной фазой. Жители населенных пунктов вблизи цементных заводов страдают от всегда висящей в воздухе тончайшей цементной пыли, образующейся при размоле цементного сырья и продукта его обжига – клинкера. Дым заводских труб, смоги, мельчайшие капельки слюны, вылетающих изо рта больного гриппом, также вредные аэролози. Аэрозоли играют важную роль в природе, быту и производственной деятельности человека. Скопление облаков, обработка полей химикатами, нанесение лакокрасочных покрытий при помощи пульверизатора, лечение дыхательных путей (ингаляция) – примеры тех явлений и процессов, где аэрозоли приносят пользу. Аэрозоли – туманы над морским прибоем, вблизи водопадов и фонтанов, возникающая в них радуга доставляет человеку радость, эстетическое удовольствие.
Для химии наибольшее значение имеют дисперсные системы, в которых средой является вода и жидкие растворы.
Природная вода всегда содержит растворенные вещества. Природные водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами. Сложные процессы жизнедеятельности, происходящие в организмах человека и животных, также протекают в растворах. Многие технологические процессы в химической и других отраслях промышленности, например получение кислот, металлов, бумаги, соды, удобрений, протекают в растворах.
КОЛЛОИДНЫЕ СИСТЕМЫ
Коллоидные системы (в переводе с греческого “колла” – клей, “еидос” вид клееподобные) – это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти частицы не видны невооруженным глазом, и дисперсная фаза и дисперсная среда в таких системах отстаиванием разделяются с трудом.
Из курса общей биологии вам известно, что частицы такого размера можно обнаружить при помощи ультрамикроскопа, в котором используется принцип рассеивания света. Благодаря этому коллоидная частица в нем кажется яркой точкой на темном фоне.
Их подразделят на золи (коллоидные растворы) и гели (студни).
1. Коллоидные растворы, или золи. Это большинство жидкостей живой клетки (цитоплазма, ядерный сок – кариоплазма, содержимое органоидов и вакуолей). И живого организма в целом (кровь, лимфа, тканевая жидкость, пищеварительные соки и т.д.) Такие системы образуют клеи, крахмал, белки, некоторые полимеры.
Коллоидные растворы могут быть получены в результате химических реакций; например, при взаимодействии растворов силикатов калия или натрия (“растворимого стекла”) с растворами кислот образуется коллоидный раствор кремниевой кислоты. Золь образуется и при гидролизе хлорида железа (III) в горячей воде.
Характерное свойство коллоидных растворов – их прозрачность. Коллоидные растворы внешне похожи на истинные растворы. Их отличают от последних по образующейся “светящейся дорожке” – конусу при пропускании через них луча света. Это явление называют эффектом Тиндаля. Более крупные, чем в истинном растворе, частицы дисперсной фазы золя отражают свет от своей поверхности, и наблюдатель видит в сосуде с коллоидным раствором светящийся конус. В истинном растворе он не образуется. Аналогичный эффект, но только для аэрозольного, а не жидкого коллоида, вы можете наблюдать в лесу и в кинотеатрах при прохождении луча света от киноаппарата через воздух кинозала.

Пропускание луча света через растворы;
а – истинный раствор хлорида натрия;
б – коллоидный раствор гидроксида железа (III).
Частицы дисперсной фазы коллоидных растворов нередко не оседают даже при длительном хранении из-за непрерывных соударений с молекулами растворителя за счет теплового движения. Они не слипаются и при сближении друг с другом из-за наличия на их поверхности одноименных электрических зарядов. Это объясняется тем, что вещества в коллоидном, т.е., в мелкораздробленном, состоянии обладают большой поверхностью. На этой поверхности адсорбируются либо положительно, либо отрицательно заряженные ионы. Например, кремниевая кислота адсорбирует отрицательные ионы SiO 3 2- , которых в растворе много вследствие диссоциации силиката натрия:

Частицы же с одноименными зарядами взаимно отталкиваются и поэтому не слипаются.
Но при определенных условиях может происходить процесс коагуляции. При кипячении некоторых коллоидных растворов происходит десорбция заряженных ионов, т.е. коллоидные частицы теряют заряд. Начинают укрупняться и оседают. Тоже самое наблюдается при приливании какого-либо электролита. В этом случае коллоидная частица притягивает к себе противоположно заряженный ион и ее заряд нейтрализуется.
Коагуляция – явление слипания коллоидных частиц и выпадения их в осадок – наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (клей, яичный белок) или при изменении кислотно-щелочной среды раствора.
2. Гели или студни представляют собой студенистые осадки, образующиеся при коагуляции золей. К ним относят большое количество полимерных гелей, столь хорошо известные вам кондитерские, косметические и медицинские гели (желатин, холодец, мармелад, торт “Птичье молоко”) и конечно же бесконечное множество природных гелей: минералы (опал), тела медуз, хрящи, сухожилия, волосы, мышечная и нервная ткани и т.д. Историю развития на Земле можно одновременно считать историей эволюции коллоидного состояния вещества. Со временем структура гелей нарушается (отслаивается) – из них выделяется вода. Это явление называют синерезисом.

Выполните лабораторные опыты по теме (групповая работа, в группе по 4 человека).
Вам выдан образец дисперсной системы. Ваша задача: определить какая дисперсная система вам выдана.
Выдано учащимся: раствор сахара, раствор хлорода железа (III), смесь воды и речного песка, желатин, раствор хлорида алюминия, раствор поваренной соли, смесь воды и растительного масла.
Инструкция по выполнению лабораторного опыта
- Рассмотрите внимательно выданный вам образец (внешнее описание). Заполните графу № 1 таблицы.
- Перемешайте дисперсную систему. Понаблюдайте за способностью осаждаться.
Осаждается или расслаивается в течении несколько минут или с трудом в течении продолжительного времени, или не осаждаются. Заполните графу № 2 таблицы.
Если вы не наблюдаете осаждение частиц, исследуйте его на процесс коагуляции. Отлейте немного раствора в две пробирки и добавьте в одну 2–3 капли желтой кровяной соли и в другую 3–5 капель щелочи, что наблюдаете?
- Пропустите дисперсную систему через фильтр. Что наблюдаете? Заполните графу № 3 таблицы. (Отфильтруйте немного в пробирку).
- Пропустите через раствор луч света фонарика на фоне темной бумаги. Что наблюдаете? (можно наблюдать эффект Тиндаля)
- Сделайте вывод: что это за дисперсная система? Что является дисперсной средой? Что является дисперсной фазой? Каковы размеры частиц в нем? (графа №5).
Правила написания синквейна :
- В первой строчке одним словом (обычно существительным) называется тема.
- Вторая строчка – это описание этой темы двумя прилагательными.
- Третья строчка – это три глагола (или глагольные формы), называющие самые характерные действия предмета.
- Четвертая строчка – это фраза из четырех слов, показывающая личное отношение к теме.
- Последняя строка – это синоним темы, подчеркивающий её суть.

Лето 2008 г. Вена. Шенбрунн.

Лето 2008 г. Нижегородская область.
Облака и их роль в жизни человека Вся окружающая нас природа – организмы
животных и растений, гидросфера и атмосфера,
земная кора и недра представляют собой сложную
совокупность множества разнообразных и
разнотипных грубодисперсных и коллоидных
систем. Краснова Мария, |
Р.S.
Огромное спасибо Першиной О.Г., учителю химии МОУ
гимназия “Дмитров”, на уроке работали с
найденной презентацией, и она дополнялась нашими
примерами.
Дисперсными называют системы, состоящие из множества малых частиц, распределенных в жидкой, твердой или газообразной среде.
Понятие «дисперсный» происходит от лат. dispersus - раздробленный, рассеянный.
Для всех дисперсных систем характерны два основных признака: высокая раздробленность (дисперсность) и гетерогенность.
Гетерогенность дисперсных систем проявляется в том, что эти системы состоят из двух (или более) фаз: дисперсной фазы и дисперсионной среды. Дисперсная фаза - это раздробленная фаза. Она состоит из частиц нерастворимого тонкоизмельченного вещества, распределенных по всему объему дисперсионной среды.
Высокая дисперсность придает веществам новые качественные признаки: повышенную реакционную способность и растворимость, интенсивность окраски, светорассеяние и т. п. Большая поверхность раздела создает в этих системах большой запас поверхностной энергии, которая делает их термодинамически неустойчивыми, чрезвычайно реакционноспособными. В них легко протекают самопроизвольные процессы, приводящие к снижению запаса поверхностной энергии: адсорбция, коагуляция (слипание дисперсных частиц), образование макроструктур и т. п. Таким образом, самые важные и неотъемлемые черты всякой дисперсной системы - гегетрогенность и высокая дисперсность - полностью определяют свойства и поведение этих систем.
Классификацию дисперсных систем проводят на основе различных признаков, а именно: по размеру частиц, по агрегатному состоянию дисперсной фазы и дисперсионной среды, по характеру взаимодействия частиц дисперсной фазы между собой и со средой.
2.2. Классификация дисперсных систем
Классификация по размеру частиц (дисперсности)
Дисперсность D является основной характеристикой дисперсной системы и мерой раздробленности вещества. Математически дисперсность определяют как величину, обратную размеру частицы:
D = 1/а ,
где а - размер частицы (диаметр или длина ребра), м -1 .
С другой стороны, для характеристики степени раздробленности служит величина удельной поверхности S уд . Удельную поверхность находят как отношение поверхности S частицы к ее объему V или массе т: S уд = S / V или S уд = S / m . Если удельную поверхность определяют по отношению к массе частицы раздробленного вещества, то ее размерность м 2 /кг, если же по отношению к объему, то размерность совпадает с размерностью дисперсности (м -1).
Физический смысл понятия «удельная поверхность» заключается в том, что это суммарная поверхность всех частиц, общий объем которых составляет 1м 3 или общая масса которых равна 1 кг.
По дисперсности системы подразделяют на типы:
1) грубо-дисперсные (грубые взвеси, суспензии, эмульсии, порошки) с радиусом частиц 10 -4 - 10 -7 м;
2) коллоидно-дисперсные (золи) с размером частиц 10 -7 - 10 -9 м;
3) молекулярные и ионные растворы с размером частиц менее 10 -9 м.
В коллоидных системах достигается высшая степень раздробления вещества, при которой еще сохраняются понятия «фаза» и «гетерогенность». Уменьшение размера частиц еще на порядок переводит системы в гомогенные молекулярные или ионные растворы.
Дисперсность влияет на все основные свойства дисперсных систем: кинетические, оптические, каталитические и т. д.
Свойства дисперсных систем сопоставлены в табл. 1.2.
Т а б л и ц а 1.2.Свойства дисперсных систем разных типов
|
Грубодисперсные |
Коллоидно-дисперсные |
Молекулярные и ионные (истинные) растворы |
|
Непрозрачные - отражают свет |
Прозрачные опалесцирующие - рассеивают свет, дают конус Тиндаля |
Прозрачные неопалесцирующие, конус Тиндаля не наблюдается |
|
Частицы не проходят через фильтр |
Частицы проходят через бумажный фильтр |
Частицы проходят через бумажный фильтр |
|
Частицы задерживаются ультрафильтрами |
Частицы проходят через льтрафильтры |
|
|
Гетерогенные |
Гетерогенные |
Гомогенные |
|
Неустойчивы кинетически и термодинамически |
Относительно устойчивы кинетически |
Устойчивы кинет. и термодинамич.ки |
|
Стареют во времени |
Стареют во времени |
Не стареют |
|
Частицы видны в оптический микроскоп |
Частицы видны в электрон. Микроскоп и ультрамикроскоп |
Частицы не видны в современные микроскопы |
Помимо размера частиц большое значение для свойств дисперсных систем имеет геометрическая форма частиц. В зависимости от условий дробления вещества форма частиц дисперсной фазы может быть очень разнообразной. Один м 3 исходного вещества принципиально возможно раздробить на кубики с длиной ребра l = 10 -8 м, вытянуть в нить с сечением 10 -8 х 10 -8 м или расплющить в пластину (пленку) толщиной 10 -8 м. В каждом из этих случаев система будет дисперсной со всеми присущими признаками.
Удельная поверхность частиц кубической формы возрастает от исходного значения в 6 м 2 до значения, определяемого по формуле
S уд = S / V = 6l 2 / l 3 = 6 . 10 8 м -1
Для нитей S уд = 4-10 8 м -1 ; для пленки S уд = 2 . 10 8 м -1 .
Частицы кубической, шарообразной или близкой к ним неправильной формы характерны для многих коллоидных растворов - золей и более грубодисперсных систем – эмульсий.
Классификация по агрегатному состоянию фаз
Наиболее распространена классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды. Каждая из этих фаз может быть в трех агрегатных состояниях: газообразном, жидком и твердом. Поэтому возможно существование восьми типов коллоидных систем (табл. 1.3). Система «газ в газе» не входит в это число, так как является гомогенной молекулярной, в ней отсутствуют границы раздела. Высокодисперсные коллоидные растворы, относящиеся к типу систем т/ж, носят название золей (от лат. solutio - раствор). Золи, у которых дисперсионной средой является вода, называют гидрозолями. Если дисперсионной средой служит органическая жидкость, коллоидный раствор носит название органозоля. Эти последние, в свою очередь, подразделяют на алкозоли, бензозоли, этерозоли и т.п., в которых дисперсионной средой являются соответственно спирт, бензол, эфир и т. д. В зависимости от агрегатного состояния дисперсионной среды различают лиозоли - золи с жидкой дисперсионной средой (от греч. lios - жидкость), аэрозоли - золи с газообразной дисперсионной средой, твердые золи - системы типа т/т. Грубодисперсные системы типа т/ж называют суспензиями, типа ж/ж – эмульсиями.
Таблица 2..2. Основные типы дисперсных систем
|
Дисп фаза |
Дисп.среда | ||
|
Не существ. |
|||
|
Жидкость |
Туман, облака, аэрозоли жидких лекарств |
||
|
Твердое тело |
Дым, пыль, порошки, аэрозоли твердых лекарств |
||
|
Жидкость |
Пены, газовые эмульсии |
||
|
Жидкость |
Эмульсии (молоко, лекарственные эмульсии) |
||
|
Твердое тело |
Суспензии, коллоидные растворы |
||
|
Твердое тело |
Твердые пены, хлеб, пемза, силикагель, активные угли |
||
|
Жидкость |
Жемчуг, капиллярные системы, цементный камень, гели |
||
|
Твердое тело |
Цветные стекла, минералы, сплавы |
Классификация по отсутствию или наличию взаимодействия между частицами дисперсной фазы
По кинетическим свойствам дисперсной фазы все дисперсные системы можно подразделить на два класса: свободно-дисперсные, в которых частицы дисперсной фазы не связаны между собой и могут свободно перемещаться (лиозоли, аэрозоли, суспензии, эмульсии), и связно-дисперсные, в которых одна из фаз структурно закреплена и не может перемещаться свободно. К этому классу относят гели и студни, пены, капиллярно-пористые тела (диафрагмы), твердые растворы и др.
Классификация по степени взаимодействия дисперсной фазы с дисперсионной средой
Для характеристики взаимодействия между веществом дисперсной фазы и жидкой дисперсионной средой служат понятия «лиофильность» и «лиофобность». Под взаимодействием фаз дисперсных систем подразумевают процессы сольватации (гидратации), т. е. образование сольватных (гидратных) оболочек из молекул дисперсионной среды вокруг частиц дисперсной фазы. Системы, в которых сильно выражено взаимодействие частиц дисперсной фазы с растворителем, называют лиофильными (по отношению к воде - гидрофильными). Если частицы дисперсной фазы состоят из вещества, слабо взаимодействующего со средой, системы являются лиофобными (по отношению к воде - гидрофобными) . Термин «лиофильный» происходит от греч. 1уо - растворяю и philia - любовь; «лиофобный» от 1уо - растворяю и phobia - ненависть, что означает «не любящий растворения». Хорошо сольватирующиеся лиофильные дисперсные системы образуются путем самопроизвольного диспергирования. Такие системы термодинамически устойчивы. Примерами таких систем являются дисперсии некоторых глин и поверхностно-активных веществ (ПАВ), растворы высокомолекулярных веществ (ВМВ).
У гидрофобных золей частицы состоят из труднорастворимых соединений, отсутствует или слабо выражено сродство дисперсной фазы к растворителю. Такие частицы плохо сольватированы. Гидрофобные золи являются основным классом коллоидных растворов, у которых ярко выражены гетерогенность и высокая удельная поверхность.